
Измерим мультиметром в режиме омметра сопротивление ограничительного резистора $R_1 = 10,1~Ом$.
Собираем измерительную цепь, состоящую из последовательно включённых батарейки, блока регулировки и шприца с раствором соли. К электродам шприца подключаем вольтметр. Второй вольтметр подключаем параллельно эталонному сопротивлению $R_1$ для измерения силы тока в цепи.
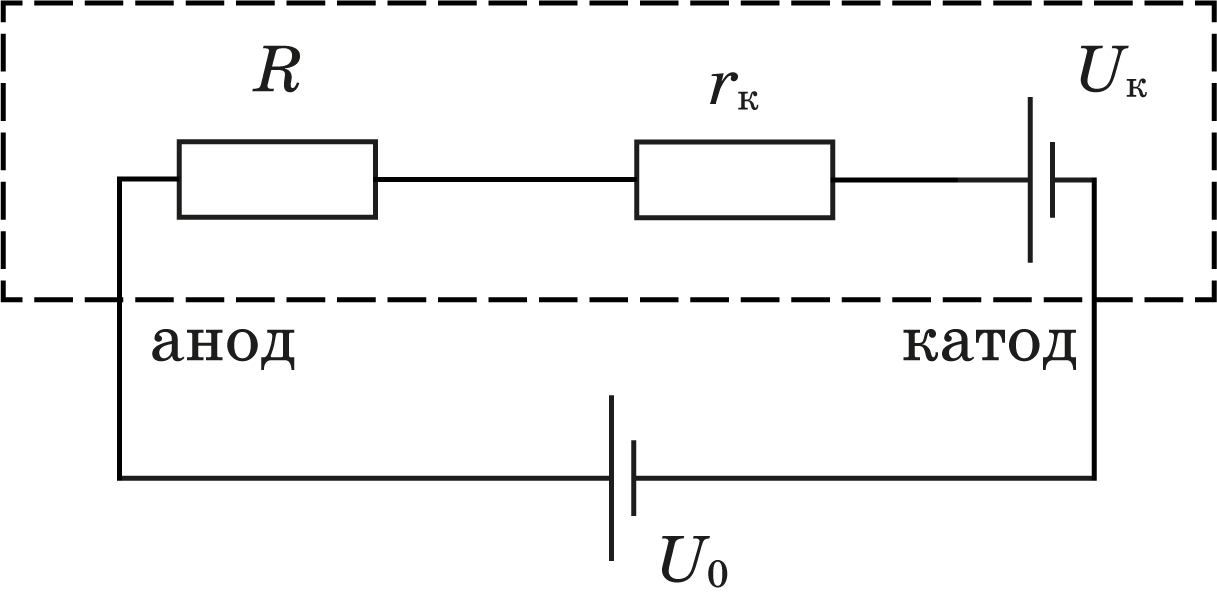
Теоретическая ВАХ электролитической ванны в рамках данной модели имеет вид
$$ I = (U - U_к) / ((\rho L/S) + r_к ) ~~~~~~~(1) $$ где $I$ – сила тока в цепи, и при фиксированной $L$ представляет собой прямую линию, пересекающую ось напряжения в точке $U = U_к$ . Коэффициент наклона этой прямой определяется суммой контактного и объёмного сопротивлений $R_{сум}$ $$(ΔU/ΔI) = (ρL/S) + r_к = R_{сум} ~~~~~~~(2) $$ Зависимость угла наклона ВАХ электролитической ванны от длины ванны $L$ в рамках данной модели, согласно $(2)$, должна быть линейной. График этой зависимости даст возможность при известной $S$ определить величины $ \rho $ и $r_к$ .
Снимаем вольт-амперную характеристику раствора. В таблицах приведены результаты измерения ВАХ раствора при 5 различных объёмах жидкости в шприце $V$ (и соответствующих расстояниях $L$ между электродами).
Строим ВАХ для всех экспериментов
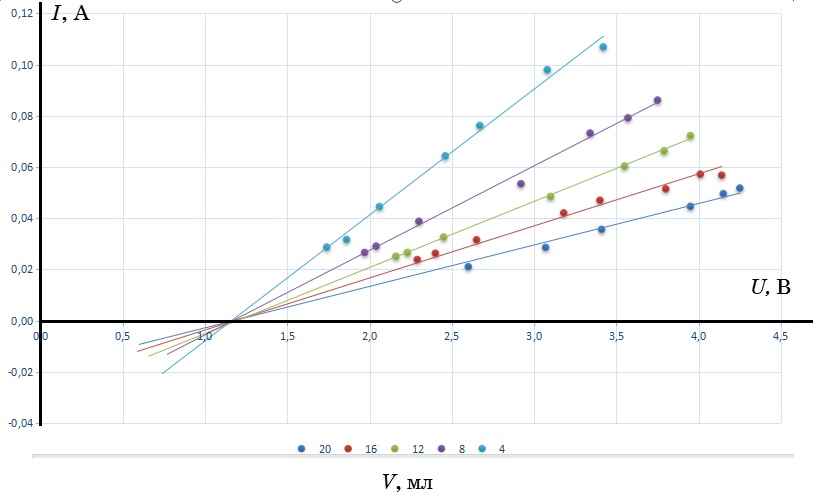
С помощью графика определяем:
1. Из точки пересечения графиков и оси напряжений величину контактной разности потенциалов $U_к = 1,2~В$.
2. Из углового коэффициента (см. формулу $(2)$) сопротивление объёма электролита вместе с сопротивлением контактных областей $R_{сум}$ для 5-ти значений $L$.
Результаты обработки экспериментальных данных для пяти значений $L$ представлены в таблице и на рисунке.
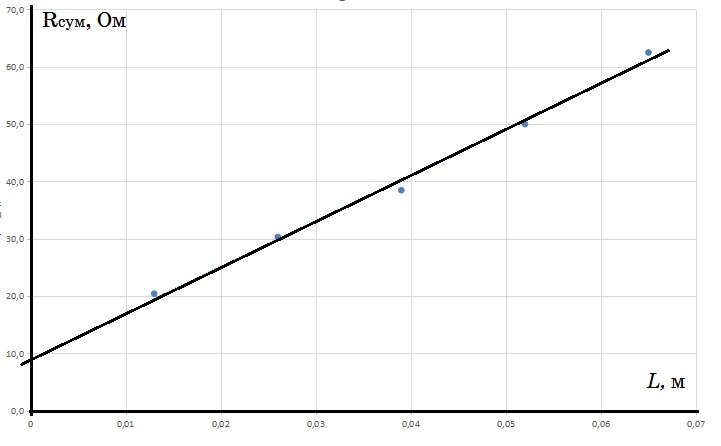
Из графика находим $r_к = R_{сум}(0) = 9,2~Ом$.
Площадь сечения поршня $S = 3,1·10^{-4}~м^2$ (можно найти измеряя диаметр поршня или отношение объёма к длине). В рамках используемой модели $ ΔR_{сум}/ΔL = ρ/S$. По наклону прямой графика $R_{сум}(L)$ находим удельное сопротивление используемого раствора соли $ρ = 0,24~ Ом·м$. То есть, $σ = 1/ρ = 4,2 ~(Ом·м)^{-1}$.
Удельная проводимость электролита $σ = 1/ρ = q_1n_1µ_1 + q_2n_2µ_2$ где $q_1$ и $q_2$ модули электрических зарядов положительных и отрицательных ионов соответственно ( в случае ионов натрия и хлора $q_1 = q_2 = е$, где $е$ – элементарный заряд), $n_1$ и $n_2$ – их концентрации ( в нашем случае они одинаковы и равны $n$), $µ_1$ и $µ_2$ - подвижности отрицательных и положительных ионов в растворе, которые, согласно условию задачи, также равны друг другу
$µ_1 = µ_2 = µ$. Окончательно, $$µ=\frac{σ}{2еn}$$
Вычисляем концентрацию ионов натрия (или хлора) в трёхпроцентном растворе поваренной соли $NaCl$ $$n =N/V=\frac{m_{NaCl}N_a\rho_{раств}}{M_{NaCl}m_{раств}}=0,03\frac{N_a\rho_{раств}}{M_{NaCl}}= 3,2·10^{26} ~м^{-3}$$.
Вычисляем подвижность: $$µ = \frac{σ}{(2еn)} = 4,0·10^{-8}\frac{м^2}{В·с}$$, что хорошо согласуется с литературными данными.