
Электролитами называют вещества, которое проводят электрический ток вследствие диссоциации на ионы. Их электропроводность обусловлена подвижностью положительно и отрицательно заряженных ионов.
Система, состоящая из ёмкости с электролитом и твердой мембраной, погруженным в него, называется электрод-электролитным интерфейсом. Такая система обладает уникальным электрическими свойствами, которые широко применяются при создании литий-ионных батарей и ионисторов (суперконденсаторов). В данной задаче мы рассмотрим основные свойства электрод-электролитного интерфейса.
В качестве электролита будет выступать раствор поваренной соли $\rm Na Cl$ в воде. В течение всей задачи будем рассматривать этот раствор, как взвесь ионов $\rm Na^+$ и $\rm Cl^-$ в жидком диэлектрике. В качестве мембраны в задаче выступает поверхность стального поршня и носика у шприца, сталь в течение всей задачи будем считать идеальным проводником, проводимость которого гораздо больше проводимости электролита.
Полезными для решения задачи могу оказаться следующие константы:
Элементарный заряд $e=1.602\cdot10^{-19}~\text{Кл}$ Число Авогадро $N_A=6.02\cdot10^{23}$ Молярная масса $\rm Na$ $\mu_{\rm Na}=23.0~\text{г}/\text{моль}$ Молярная масса $\rm Cl$ $\mu_{\rm Cl}=35.4~\text{г}/\text{моль}$ Молярная масса $\rm H$ $\mu_{\rm H}=1.0~\text{г}/\text{моль}$ Молярная масса $\rm O$ $\mu_{\rm O}=16.0~\text{г}/\text{моль}$
Внимание! В задаче не требуется оценка погрешностей.
Внимание! Пользуйтесь индивидуальной лампой для освещения рабочего места.
Оборудование:

В рамках задачи будем обозначать концентрацию раствора соли в воде безразмерной величиной $c = \dfrac{m_\text{соли}}{m_\text{воды}}$, где $m_\text{воды}$ — масса изначально взятой чистой воды, $m_\text{соли}$ — масса порошка соли, добавленного к чистой воде для получения раствора.
Приготовьте раствор соли с концентрацией $c\approx 0.07$. Наберите этот раствор в шприц, причем, чтобы избежать образования лишних пузырей внутри шприца, двигайте поршень медленно. При измерениях нужно держать шприц в каком-то фиксированном положении (например, стоящим на ножке поршня), чтобы конфигурация пузырей, которые так или иначе образуются, была одинаковой.


В течение всей задаче мы будем изучать электрические свойства раствора электролита внутри шприца, поэтому следует использовать схему, изображенную на рисунке.
Внимание! Осциллографические провода и провода генератора ни в коем случае не должны непосредственно касаться стеклянного шприца, если Вы в него уже набирали воду.
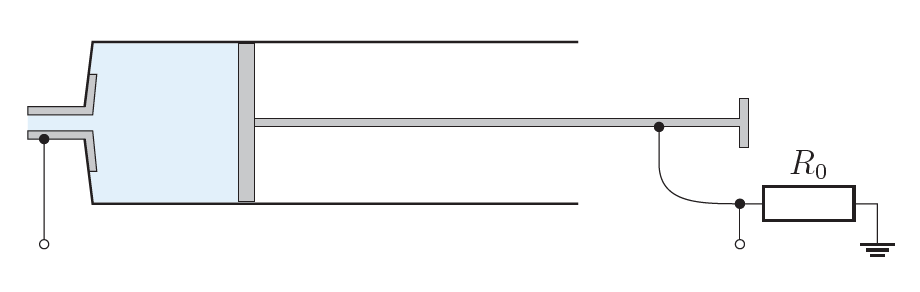
Используйте генератор в режиме $V_{\text{pp}}=1.00~\text{В}$, где $V_\text{pp}$ — разность напряжений между пиками (двойная амплитуда сигнала). Обязательно не забудьте включить сигнал на выходе генератора:
Ток в нашей системе может значительно зашумлен (это т.н. электрохимический шум, который симметричен в положительную и в отрицательную область), поэтому любые амплитуды напряжений стоит измерять в режиме Cursor в ручном режиме и не полагаться на модуль Measure.
Для измерения напряжения на шприце обязательно получайте его в виде сигнала с помощью модуля Math в режиме вычитания.
Для работы с модулем Math:
Когда все настроено, и Вы находитесь в другом окне, например Cursor, для изменения масштаба канала Math выполните пункты 1 и 2, а затем регулируйте масштаб той же ручкой, что меняется масштаб обычных каналов (Vertical Scale).
Проверьте, что для каналов CH1 и CH2 настройка «Пробник» соответствует режиму пробника, в котором используется щуп. Если не соответствует, то настройте.

При частоте $f\approx50~\text{кГц}$ разность фаз между током через шприц и напряжением на нем практически равна нулю. Это означает, что при этой частоте раствор электролита внутри шприца ведет себя, как сопротивление $R$. Стоит ожидать, что это сопротивление меняется при изменении длины $L$ электролита внутри шприца.
Приготовьте 4 разных раствор соли с концентрациями $0.07 \leq c \leq 0.20$. При смене концентрации раствора внутри шприца обязательно промойте его чистой водой.
Теоретическое описание полученных результатов следует из стандартной задачи проводимости второго рода: рассмотрим действие электрического поля на заряженную частицу в вязкой среде. Пусть масса частицы $m$, а заряд $q$, а если частица движется, то на нее действует сила вязкого трения $F=-kv$.
Коэффициент вязкости $k$, с помощью которого мы моделируем движение ионов в растворе связан не только с вязкостью, но и с электрическими свойствами воды и зависит от концентрацией ионов:
\[ k \propto n^{\alpha}, \]
где $\alpha$ — неизвестная степень, одинаковая для ионов $\rm Na^+$ и $\rm Cl^-$.
Пусть электронейтральный раствор поваренной соли находится внутри цилиндрического сосуда с проводящими основаниями-электродами и непроводящими стенками. Площадь оснований $S$, расстояние между ними $L$. Будем считать, что ионы $\rm Na^+$ и $\rm Cl^-$ в любом количестве могут возникать и пропадать в результате химических реакций с электродами. Заряды ионов по модулю совпадают с элементарным зарядом $e=1.602\cdot10^{-19}~\text{Кл}$.
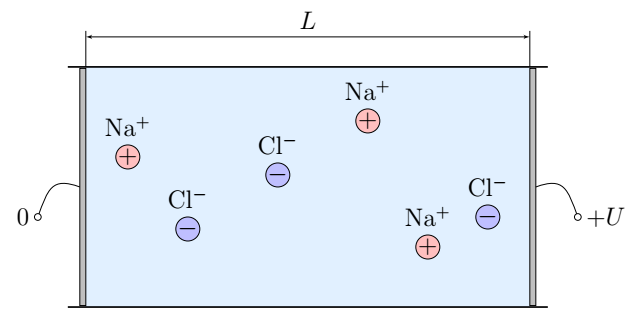
Обозначим за $n$ концентрацию ионов натрия, за $k_{\rm Na^+}$ и $k_{\rm Cl^-}$ — коэффциенты взякости для ионов натрия и хлора соотвественно.
На практике исследование постоянного тока сопряжено со следующей трудностью: из-за химических реакций постепенно разрушаются/покрываются пленкой основания цилиндра. Поэтому значительно удобнее исследовать проводимость при переменном токе. Проведем теоретический анализ в рамках нашей модели.
B6
0.25
Теперь учтем поверхностные эффекты в виде резистора $R_\text{п}$, который последовательно подключен к раствору. Запишите формулу для импеданса $\tilde{Z}(\omega)$ системы, состоящей из раствора $\rm NaCl$ и сосуда. Ответ запишите через $n,S,L,e,m_{\rm Na^+}, m_{\rm Cl^-},\omega,k_{\rm Na^+}, k_{\rm Cl^-}$ и $R_\text{п}$.
Случаю, рассмотренному в $\textbf{B8}$ очевидно соответствуют измерения, сделанные в рамках пунктов $\textbf{A2}$ и $\textbf{B1}$.
Полученное в эксперименте $\mu_\text{эфф}$ значительно отличается от теоретического значения. Это отличие можно объяснить тем, что молекулы воды, которые обладают дипольным моментом, притягиваются к ионам (сольватируют их) и двигаются вместе с ними. Обозначим, количество молекул воды, двигающихся вместе с ионом любого вида за $N$.
В таком случае вместо $\mu_{\rm Na}$ при расчете нужно использовать $\mu_{\rm Na}+N\mu_{H_2O}$ и вместо $\mu_{\rm Cl}$ нужно использоваться $\mu_{\rm Cl} + N \mu_{H_2O}$
Шприц с электролитом также обладает ёмкостью, которую невозможно предсказать в рамках теории объемных эффектов. Эта ёмкость начинает сказываться при малых частотах сигнала, подаваемого на концы шприца.
Ёмкость системы поверхность электрода-электролит связана с тем, что ионы(как и любые заряженые частицы) притягиваются к поверхности металла и формируют т.н. двойной электрический слой. Таким образом единица поверхности соприкосновения металла с электролитом обладает ёмкостью $\sigma = \frac{dC}{dS}$, где $C$ — ёмкость поверхности площадью $S$.
Наполните шприц раствором с концентрацией соли $c\approx 0.20$.
Для анализа электрической схемы бывает полезна т.н. диаграмма Найквиста — зависимость $\mathfrak{Im} \tilde{Z}$ от $\mathfrak{Re} \tilde{Z}$.
В нашем случае можно считать, что объемные эффекты сводятся к резистору сопротивлением $R_2$, а поверхностные выражаются из измерений следующим образом: $\tilde{Z}_\text{п} = \tilde{Z} - R_2$.
Описанная ранее модель формирования ёмкости $C$ у поверхности соприкосновения электролита и металла в случае, если эта поверхность плоская, должна сводится к тому, что поверхностные эффекты имеют диаграмму Найквиста, как у конденсатора, но эксперимент противоречит этому тезису. При анализе схожей задачи датским химиком Робертом де Леви была предложена модель шероховатой поверхности металла, которая оказалась очень плодотворной для описания электрических свойств электрод-электролитных интерфейсов.
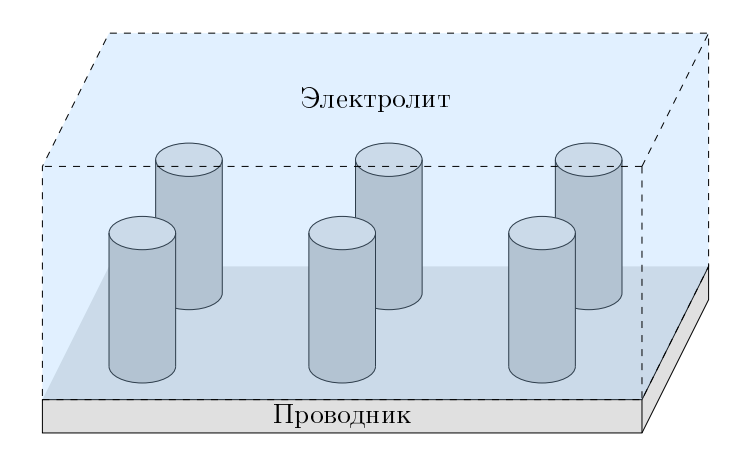
Представим поверхность проводника, как плоскость, на которой стоят цилиндры высоты $l$ и радиуса $r$. Плотность постановки цилиндров можно описать поверхностной плотностью $\xi = \frac{dN}{dS}$, где $N$ — число цилиндров на площади $S$.
В таком случае на один цилиндр приходится $1/\xi$ площади электролита вокруг него. При этом единица высоты цилиндра обладает некоторой ёмкостью $C_l$ и единица высоты электролита, приходящегося на один цилиндр, обладает некоторым сопротивлением $R_l$. Для сокращения записей обозначим за $\rho$ удельное сопротивление электролита.
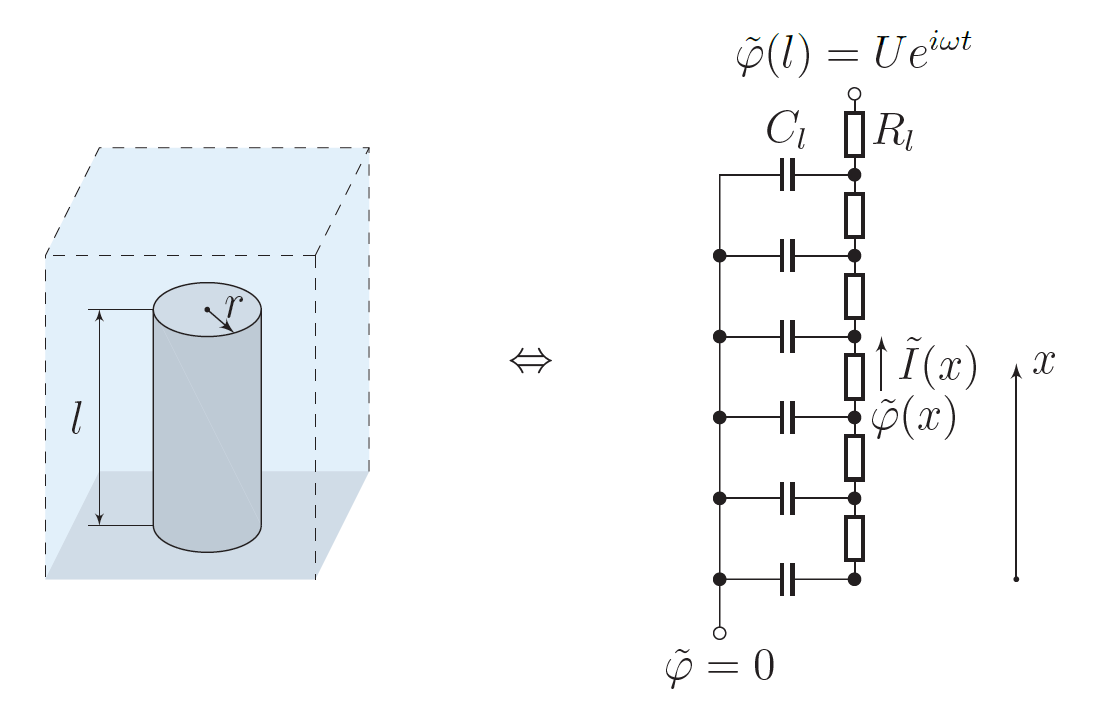
Примечание 1: для нахождения двух чисел $a$ таких, что $a^2=\sqrt{i}$ можно воспользоваться формулой Эйлера.
Примечание 2: $\cos x = \cosh ix$, $i \sin x = \sinh ix$, $i \tan x = \tanh ix$, $\tanh(x \pm y) = \dfrac{\tanh x \pm \tanh y}{1 \pm \tanh x \tanh y}$.
C8
1.25
Решите полученную в пунктах $\textbf{C5}$ и $\textbf{C6}$ систему дифференциальных уравнений и получите импеданс $\tilde{Z}_\text{ц}(\omega)$ одного цилиндра и электролита, окружающего его. Ёмкостью основания цилиндра и ёмкостью плоской поверхности, на которой стоят цилиндры пренебрегайте. Ответ выразите через $C_l,R_l,l$ и $\omega$.
C10
0.20
Чему равен импеданс $\tilde{Z}_\text{п}(\omega)$ одной поверхности цилиндра, соприкасающейся с электролитом. Площадь поверхности $S$. Ответ выразите через $r,\sigma,\rho,\xi,S$ и $\omega$.
Нарисуйте качественно диаграмму Найквиста $\tilde{Z}_\text{п}(\omega)$. Теоретическая и экспериментальная диаграммы Найквиста должны совпадать по форме, но часть их характеристик могут незначительно отличаться.
Будем считать, что $\xi=40~\frac{1}{\text{мм}^2}$, $r=0.6~\text{мкм}$. Площадь контакта носика шприца с электролитом считайте в $5.5$ раз меньше площади внутреннего сечения шприца.